Maladies auto-immunes : comprendre les mécanismes de dérégulation immunitaire
Introduction
Fatigue persistante, douleurs diffuses, troubles digestifs, brouillard mental ou inflammation chronique…. Bien que les maladies auto-immunes regroupent des pathologies aux expressions cliniques variées, elles partagent un socle commun : un système immunitaire qui perd sa capacité à distinguer le « soi » (nos propres cellules) du « non-soi » (les agresseurs extérieurs).
Normalement, notre système immunitaire est un réseau de surveillance biologique très complexe chargé de nous protéger des bactéries, virus et toxines. Chez certaines personnes, cet équilibre se rompt. Le système peut alors devenir excessivement réactif, entretenir une inflammation chronique ou diriger ses attaques contre les tissus de l’organisme lui-même. C’est le cas dans la polyarthrite rhumatoïde, la sclérose en plaques, la thyroïdite d’Hashimoto ou le lupus.
Au-delà de l'atteinte physique, le caractère "invisible" de ces symptômes (comme l'épuisement profond ou le brouillard mental) constitue un défi psychologique majeur, car il est souvent difficile de faire comprendre à son entourage une souffrance qui ne se voit pas à l’œil nu
Cet article explore les interactions complexes entre génétique, environnement, microbiote et système nerveux qui sous-tendent ces dérégulations.
1) Le système immunitaire : un équilibre extrêmement précis
Le rôle du système immunitaire dépasse la simple « attaque » des microbes. Sa fonction première est d'apprendre la tolérance immunitaire. Chaque jour, l'organisme produit des millions de cellules capables de détecter des intrus ou des cellules anormales, mais elles doivent impérativement apprendre à ignorer les constituants sains de l’organisme. Cette tolérance n’est pas passive : elle repose sur des mécanismes actifs de régulation et de freinage de la réponse immunitaire.
Lorsque cette tolérance est optimale, l’inflammation est un processus temporaire et contrôlé. Si les mécanismes de régulation faiblissent, des cellules deviennent auto-réactives, transformant une réponse de protection en une auto-immunité pathologique.
Le système immunitaire repose normalement sur un équilibre subtil entre défense contre les agressions extérieures et tolérance envers les constituants de l’organisme.
Voici une représentation simplifiée de cet équilibre et des mécanismes pouvant conduire à une dérégulation auto-immune (cliquez sur l'image pour l'agrandir) :
Cette rupture d’équilibre ne dépend probablement jamais d’un seul facteur isolé.
Les maladies auto-immunes résultent plutôt d’interactions complexes entre terrain génétique, environnement, inflammation, microbiote, infections et système nerveux.
2) Pourquoi le système immunitaire peut-il se dérégler ?
Les maladies auto-immunes sont multifactorielles ; il n'existe pas de cause unique. On observe plutôt une interaction progressive entre plusieurs facteurs de risque :
- Le terrain génétique.
- L'environnement et les toxines.
- Les infections passées ou chroniques.
- La dysbiose et l'hyperperméabilité intestinale.
- Le stress chronique et les dérégulations hormonales (cortisol).
Chez une personne prédisposée, la rencontre de plusieurs de ces facteurs peut déclencher la rupture de l’équilibre immunitaire.
3) Le rôle du terrain génétique et du système HLA
Le système HLA (Human Leukocyte Antigen) est l'un des éléments les plus étudiés. Il s'agit de marqueurs à la surface de nos cellules qui font office de « carte d’identité biologique ». Ils permettent au système immunitaire d'identifier instantanément si une cellule lui appartient.
Certaines variantes HLA sont associées à une vulnérabilité accrue, comme par exemple :
- HLA-B27 pour la spondylarthrite ankylosante.
- HLA-DR pour la polyarthrite rhumatoïde.
Posséder ces gènes ne signifie pas que la maladie se déclarera, mais cela définit un terrain de susceptibilité où l'organisme pourrait réagir plus vivement à certains stimuli environnementaux.
L'épigénétique : pourquoi nos gènes ne sont pas notre destin
Si la génétique "charge le pistolet", c’est bien souvent l’environnement et notre mode de vie qui "appuient sur la détente".
C’est tout le principe de l’épigénétique : nos gènes ne sont pas une condamnation figée, mais un code dont l'expression peut varier.
En agissant sur nos piliers de santé, comme la qualité de l’alimentation, la gestion du stress ou la réduction de l'exposition aux toxines, nous avons le pouvoir d'influencer positivement la manière dont nos gènes s'expriment, ouvrant ainsi la voie à un retour progressif vers l’équilibre.
4) Inflammation chronique et dérégulation immunitaire
L’inflammation chronique joue un rôle central dans l'entretien de l'auto-immunité. Elle est orchestrée par des messagers chimiques appelés cytokines pro-inflammatoires (TNF-α, IL-1, IL-6, interféron gamma), tels que présentés dans l'article : Comprendre les cytokines et les cellules : le langage secret de l’immunité
L’inflammation repose sur une communication permanente entre différentes cellules immunitaires grâce à des messagers chimiques appelés cytokines.
Certaines favorisent l’activation inflammatoire, tandis que d’autres participent à limiter et à résoudre cette réponse.
Lorsque cet équilibre devient instable ou prolongé dans le temps, l’inflammation peut perdre son rôle protecteur initial et contribuer progressivement à certaines dérégulations chroniques (voir l’article : Maladie de Lyme : pourquoi certains symptômes peuvent-ils persister ?).
Normalement, des cytokines anti-inflammatoires viennent limiter cette réponse. Si cet équilibre se rompt, l'inflammation devient un état permanent qui endommage les tissus et maintient le système immunitaire en hyperactivation. Ce feu invisible augmente le stress oxydatif, ce qui perturbe les mitochondries (nos centres de production d’énergie cellulaire) et épuise les capacités d'adaptation de l’organisme. Ces mécanismes sont détaillés dans l’article consacré : Les cellules humaines : énergie, inflammation, stress oxydatif et récupération
5) Le microbiote intestinal : une interface majeure avec l’immunitée
L’intestin abrite la majorité de nos cellules immunitaires. Une dysbiose (déséquilibre du microbiote) est fréquemment observée dans les pathologies auto-immunes.
Le microbiote intestinal, la barrière digestive et le système immunitaire échangent en permanence des signaux chimiques et immunitaires.
Cet équilibre joue un rôle majeur dans la régulation de l’inflammation et des capacités de tolérance immunitaire.
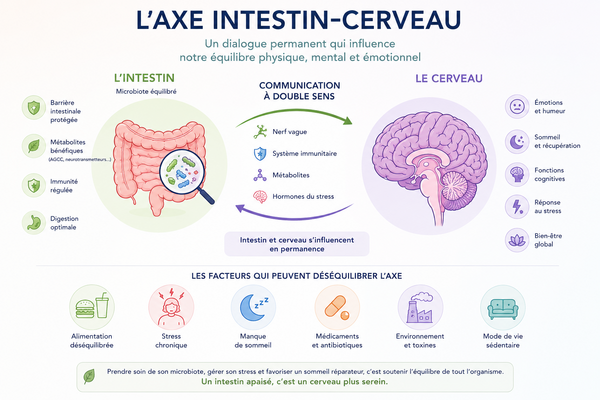
Lorsque cet équilibre est perturbé, certaines hypothèses suggèrent qu’une activation immunitaire excessive pourrait progressivement contribuer à entretenir certains terrains inflammatoires chroniques. Une partie de ces interactions est détaillée dans l’article : Axe intestin-cerveau : microbiote, stress, sommeil et émotions
L'hypothèse de l'hyperperméabilité intestinale suggère que lorsque la barrière intestinale est fragilisée, des fragments microbiens ou des molécules alimentaires peuvent passer dans le sang. Cela pourrait contribuer à stimuler de manière inappropriée le système immunitaire, entretenant l'inflammation et les dérégulations auto-immunes.
6) Stress chronique, système nerveux et immunité
Le stress chronique ne se limite pas à une sensation psychologique.
Il modifie également le fonctionnement hormonal, nerveux et immunitaire, notamment à travers le cortisol, hormone centrale de l’adaptation au stress.
Lorsque cette activation devient prolongée, l’organisme peut progressivement perdre une partie de ses capacités naturelles de récupération, favorisant fatigue, troubles du sommeil, inflammation chronique et hypersensibilité physiologique.
Le système immunitaire interagit en permanence avec le cerveau et le système nerveux. Le stress prolongé et le cortisol influencent directement la production de cytokines et l'activité inflammatoire.
Cette hypervigilance physiologique maintient le système nerveux autonome dans un état d'alerte, ce qui favorise la fatigue, les troubles du sommeil et les douleurs diffuses. On ne peut donc pas accompagner l'immunité sans apaiser le système nerveux. Pour en savoir davantage, consultez les articles :
7) Infections et auto-immunité : des interactions complexes
Certaines infections virales, telles que EBV (Epstein-Barr Virus) , zona, hépatite C, sont suspectées de déclencher ou d'aggraver l'auto-immunité. Le mécanisme principal est le mimétisme moléculaire : certaines protéines du virus ressemblent tellement à nos propres tissus que le système immunitaire, en voulant attaquer le virus, finit par attaquer l'organisme par erreur.
Cette hypothèse suggère que certains fragments microbiens pourraient présenter des ressemblances avec certaines structures de l’organisme, favorisant parfois des réactions immunitaires croisées.
Ce mécanisme ne semble probablement concerner qu’une partie des personnes génétiquement ou immunologiquement prédisposées. Les maladies auto-immunes résultent probablement d’interactions beaucoup plus complexes entre terrain génétique, immunité, inflammation, microbiote, environnement et infections.
8) Pourquoi les symptômes sont-ils souvent généralisés ?
Même si une maladie cible un organe précis (thyroïde, articulations), l’inflammation qu'elle génère circule partout. Cela impacte la production d’énergie cellulaire et le sommeil, expliquant pourquoi les patients décrivent souvent une « inflammation généralisée », un brouillard mental et une fatigue profonde qui dépasse largement le cadre de l'organe touché.
Cette inflammation chronique peut également perturber les mitochondries et réduire progressivement les capacités de production d’énergie cellulaire.
9) Approches complémentaires : soutenir le terrain
Face à ces dérégulations complexes, les approches complémentaires ne visent pas à “supprimer” le système immunitaire, mais plutôt à soutenir les capacités naturelles d’adaptation, de récupération et d’équilibre de l’organisme.
9.1) Modes de vie et récupération
L'accompagnement naturel ne remplace jamais le traitement médical, mais vise à restaurer les capacités de récupération de l’organisme. Le sommeil, l’activité physique adaptée et la stabilité glycémique jouent également un rôle important dans les capacités de récupération et de régulation inflammatoire.
Dans ces contextes inflammatoires complexes, l’objectif n’est pas de “forcer” l’organisme, mais plutôt de restaurer progressivement ses capacités naturelles d’adaptation, de récupération et d’équilibre.
9.2) Micronutrition et mode de vie
La micronutrition joue un rôle de "modulateur" : elle apporte aux cellules les outils nécessaires pour freiner l'inflammation et réparer les tissus lésés. Voici les piliers essentiels pour accompagner un terrain auto-immun :
La Vitamine D : un acteur important de la régulation immunitaire
Bien plus qu'une simple vitamine pour les os, la Vitamine D agit comme une véritable hormone immunomodulatrice. Elle aide le système immunitaire à produire des cellules T-régulatrices (T-regs), dont le rôle est précisément de calmer les réponses immunitaires excessives et d'éviter que le corps ne s'attaque à lui-même. Un statut satisfaisant en vitamine D est aujourd’hui étudié dans de nombreux contextes inflammatoires et auto-immuns.
Les Oméga-3 (EPA et DHA) : des acteurs importants de la résolution de l’inflammation
Ces acides gras essentiels s'insèrent dans la membrane de nos cellules (voir Chapitre 2 sur la cellule). Ils servent de précurseurs à des molécules appelées résolvines, qui ont pour mission de "résoudre" l'inflammation, c'est-à-dire d'y mettre fin activement plutôt que de simplement la masquer. Ils permettent ainsi de limiter la production de cytokines pro-inflammatoires.
Le Magnésium : Le bouclier anti-stress et énergétique
Le stress est un déclencheur majeur de poussées auto-immunes. Or, le stress consomme énormément de magnésium, et le manque de magnésium rend plus vulnérable au stress : c'est un cercle vicieux (voir l'article : Stress : comprendre les mécanismes et les solutions naturelles)
Il est indispensable pour stabiliser le système nerveux et soutenir les mitochondries, qui sont souvent épuisées chez les patients souffrant de fatigue chronique liée à l'auto-immunité.
Le Zinc et le Sélénium : Protection et barrière
- Le Zinc est vital pour l'intégrité des "jonctions serrées" de l'intestin. Le Zinc participe notamment au maintien de l’intégrité des jonctions serrées intestinales.
- Le Sélénium est un puissant antioxydant, particulièrement crucial dans les pathologies thyroïdiennes (comme Hashimoto), car il aide à neutraliser le stress oxydatif produit lors de la synthèse des hormones.
La L-Glutamine et les Polyphénols : Réparer l'interface
Pour refermer les "portes" de l'intestin, la L-glutamine est largement étudiée pour son rôle de soutien des entérocytes, les cellules de la paroi intestinale.
Certains polyphénols (issus du thé vert, du curcuma ou des petits fruits rouges) semblent également influencer favorablement l’équilibre du microbiote intestinal.
Les besoins micronutritionnels pouvant varier fortement selon les personnes et les pathologies, ces approches nécessitent idéalement un accompagnement individualisé.
9.3) Accompagnement aromatique (HE)
Les huiles essentielles n’ont pas vocation à remplacer une prise en charge médicale des maladies auto-immunes. Cependant, certaines molécules aromatiques présentent des propriétés biologiques documentées qui peuvent être intéressantes dans une approche de terrain : modulation de certaines voies inflammatoires, soutien neurovégétatif, confort digestif, détente nerveuse, accompagnement du sommeil ou des douleurs :
Apaiser le système nerveux (Esters)
La Lavande vraie ou le Petit grain bigarade sont riches en esters et en linalol. Ils agissent via l'olfaction pour lever l'hypervigilance nerveuse et favoriser un sommeil réparateur, essentiel à la régulation immunitaire
Accompagner la sensibilité inflammatoire (Sesquiterpènes)
Certaines molécules, comme le β-caryophyllène, sont étudiées pour leurs interactions avec des voies impliquées dans l’inflammation, le stress oxydatif et la régulation neuro-immunitaire. On le retrouve notamment dans le Copaïba, mais aussi dans le Poivre noir, l’Ylang-ylang, les feuilles de Katafray, la Maniguette ou les feuilles de Goyave, …
Confort digestif (Phénols/Oxydes en douceur)
Le Gingembre aide à soutenir la digestion lente, parfois observée dans ces contextes de stress.
Confort musculaire et articulaire (Monoterpènes / Sesquiterpènes)
Certaines huiles essentielles traditionnellement utilisées pour le confort musculaire et articulaire peuvent également être intéressantes dans les contextes inflammatoires chroniques, notamment lorsque douleurs diffuses, tensions ou hypersensibilités sont présentes.
Parmi les huiles essentielles souvent utilisées dans cette optique figurent par exemple le Katafray (écorce), la Gaulthérie odorante, l’Eucalyptus citronné, le Genévrier ou encore certaines huiles riches en β-caryophyllène
Ancrage émotionnel (Sesquiterpénols)
L'Encens est traditionnellement utilisé pour accompagner les états de fatigue nerveuse profonde et aider à la « déconnexion » du mode alerte.
À retenir
L’équilibre immunitaire dépend d’une communication permanente entre nos cellules, notre intestin et notre système nerveux. Comprendre ces mécanismes permet de saisir l'importance capitale du sommeil, du microbiote et de la gestion du stress dans le maintien des capacités naturelles d’équilibre et de récupération de l’organisme.
Dans ces contextes complexes, l’objectif n’est pas de rechercher une solution unique, mais plutôt de restaurer progressivement les capacités naturelles d’équilibre, de récupération et d’adaptation de l’organisme.
Note importante : Cet article est purement informatif et ne remplace pas l'avis d'un médecin. Toute utilisation d'huiles essentielles doit être encadrée, surtout en cas de pathologie chronique.